1️⃣ Карбоновые кислоты изменяют окраску индикаторов: лакмус и метилоранж становятся ❤️
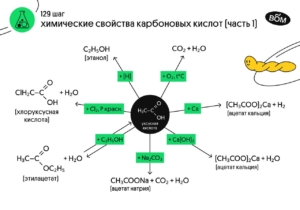
2️⃣ Взаимодействие с металлами, стоящими в ЭХР до водорода
2СH₃COOH + Ca → (СH₃COO)₂Ca + H₂
3️⃣ Взаимодействие с основаниями. Эта реакция является реакцией нейтрализации
СH₃COOH + NaOH → СH₃COONa + H₂O
4️⃣ Взаимодействие с основными и амфотерными оксидами
2СH₃COOH + CaO → (СH₃COO)₂Ca + H₂O
5️⃣ Взаимодействие с солями угольной кислоты (более слабой и летучей)
СH₃COOH + NaHCO₃ → СH₃COONa + CO₂ + H₂O
6️⃣ Галогенирование
Условие: красный фосфор
СH₃COOH + Сl₂ → ClСH₂COOH + HCl (P кр.)
❗️Замещение происходит в альфа-положение
7️⃣ Реакция этерификации
Условие: t°C, H⁺
СH₃OH + СH₃СOOH → СH₃СOOСH₃ + H₂O (t°C, H⁺)
Образуются сложные эфиры. Реакция обратима.
❗️От спирта отщепляется -H, от кислоты -OH
8️⃣ Взаимодействие с PCl₅ и PCl₃ с образованием хлорангидридов
СH₃СOOH + PCl₅ → СH₃СOСCl + POCl₃ + HCl
СH₃СOOH + PCl₃ → СH₃СOСCl + H₃PO₃
Эти реакции вряд ли попадутся во второй части, но для первой могут пригодиться 🤓
9️⃣ Восстановление
Действием сильных восстановителей (например, LiAlH₄) можно восстановить кислоты до альдегидов или спиртов.
Такие реакции для ЕГЭ знать не нужно!
1️⃣0️⃣ Горение (полное окисление)
Условие: t°C
СH₃СOOH + 2O₂ → 2CO₂ + 2H₂O (t°C)
🔸 НЕПРЕДЕЛЬНЫЕ КИСЛОТЫ
В составе таких кислот содержится одна или несколько кратных связей со всеми вытекающими отсюда последствиями!
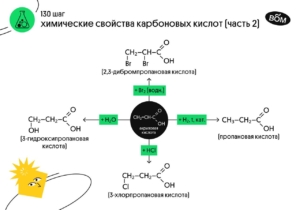
Это значит, что непредельные кислоты могут вступать в реакции присоединения по кратной связи и обесцвечивать бромную воду!
СH₂=CHСOOH + Br₂ → Br-СH₂-CH(Br)-СOOH
⠀
❗️Присоединение HCl или H₂O к акриловой кислоте протекает против правила Марковника (из-за наличия электроноакцепторной -СOOH группы)
СH₂=CHСOOH + HCl → Cl-СH₂-CH₂-СOOH
⠀
Непредельные кислоты можно гидрировать (присоединять водород):
СH₂=CHСOOH + H₂ → СH₃-CH₂-СOOH (t°C, Ni)
⠀
🔸 МУРАВЬИНАЯ КИСЛОТА
HCOOH — простейший представитель карбоновых кислот. Обратите внимание на строение этой молекулы, она содержит как будто и карбоксильную, и карбонильную группу 😱
Благодаря этому, муравьиная кислота вступает в реакции, нехарактерные для карбоновых кислот, но характерные для альдегидов!
⠀
Она легко окисляется:
1️⃣ перманганатом калия в кислой среде
5HCOOH + 2KMnO₄ + 3H₂SO₄ → 5CO₂ + 2MnSO₄ + K₂SO₄ + 8H₂O
⠀
2️⃣ аммиачным раствором оксида серебра
HCOOH + 2[Ag(NH₃)₂]OH → (NH₄)₂CO₃ + 2Ag + 2NH₃ + H₂O
⠀
3️⃣ гидроксидом меди(II)
HCOOH + Cu(OH)₂ → 2CO₂ + 3H₂O + Cu₂O (t°C)
⠀
Под действием концентрированной серной кислоты распадается:
HCOOH → CO + H₂O (H₂SO₄)
Авторизуйтесь, чтобы оставить комментарий.