Разбираем задания с Дальнего Востока ЕГЭ 2025 по химии!
Задание 31: Дальний Восток ЕГЭ 2025
Образец нитрата натрия прокалили. Образовавшийся твердый остаток разделили на три части. Первую поместили в раствор, содержащий иодид натрия и серную кислоту. Вторую добавили к раствору хлорида аммония и нагрели. Третью поместили в нейтральный раствор перманганата калия, при этом выделялся бурый осадок.
1) 2NaNO₃ = 2NaNO₂ + O₂
2) 2NaNO₂ + 2NaI + 2H₂SO₄ = 2Na₂SO₄ + 2NO + I₂ + 2H₂O
3) NaNO₂ + NH4Cl = NaCl + N₂ + 2H2O
4) 3NaNO₂ + 2KMnO₄ + H₂O =2MnO₂ + 3NaNO₃ + 2KOH
Задание 31: Дальний Восток ЕГЭ 2025
Железо прокалили с серой. Продукт реакции растворили в соляной кислоте. Через раствор
полученной соли пропустили хлор. К образовавшемуся веществу добавили избыток раствора
сульфида калия, при этом выделения газа не наблюдалось.
1) Fe + S FeS
2) FeS + 2HCl = FeCl₂ + H₂S
3) 2FeCl₂ + Cl₂ = 2FeCl₃
4) 2FeCl₃ + 3K₂S = 2FeS + S + 6KCl
Задания 29-30: Дальний Восток ЕГЭ 2025
Вещества: карбонат аммония, иодид калия, серная кислота, перманганат калия, ацетат кальция и пероксид водорода.
ОВР: образуется щёлочь, два нерастворимых вещества, газ не выделяется
2KMnO₄ + 6KI + 4H2O = 3I₂ + 2MnO₂ + 8KOH
РИО: образуется осадок
(NH₄)₂CO₃ + (CH₃COO)₂Ca = 2CH₃COONH₄ + CaCO₃
(не забывайте, осадки не расписываем на ионы!)
Задания 29-30: Дальний Восток ЕГЭ 2025
Вещества: сульфид калия, гидрокарбонат калия, серная кислота, хлорид натрия, перманганат натрия, хлорид натрия.
ОВР: образуется два нерастворимых вещества
2NaMnO₄ + 3Na₂S + 4H₂O = 2MnO₂ + 3S + 8NaOH (c сульфидом натрия)
2NaMnO₄ + 3K₂S + 4H₂O = 2MnO₂ + 3S + 2NaOH + 6KOH (c сульфидом калия)
РИО: в реакцию вступает кислая соль
2KHCO₃ + H₂SO₄ = K₂SO₄ + 2CO₂ + 2H₂O
Воду и CO₂ не расписываем на ионы!
KHCO₃ = K⁺ + HCO₃⁻
Задание 33: Дальний Восток ЕГЭ 2025
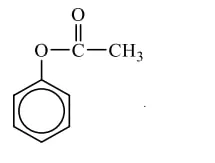
Данное вещество подвергается гидролизу под действием гидроксида натрия с образованием двух солей.
Простейшая формула: C₄H₄O
Молекулярная формула: C₈H₈O₂
При гидролизе сложного эфира образуется две соли, если эфир образован фенолом! Тогда загадан фенилацетат.
Задание 32: Дальний Восток ЕГЭ 2025
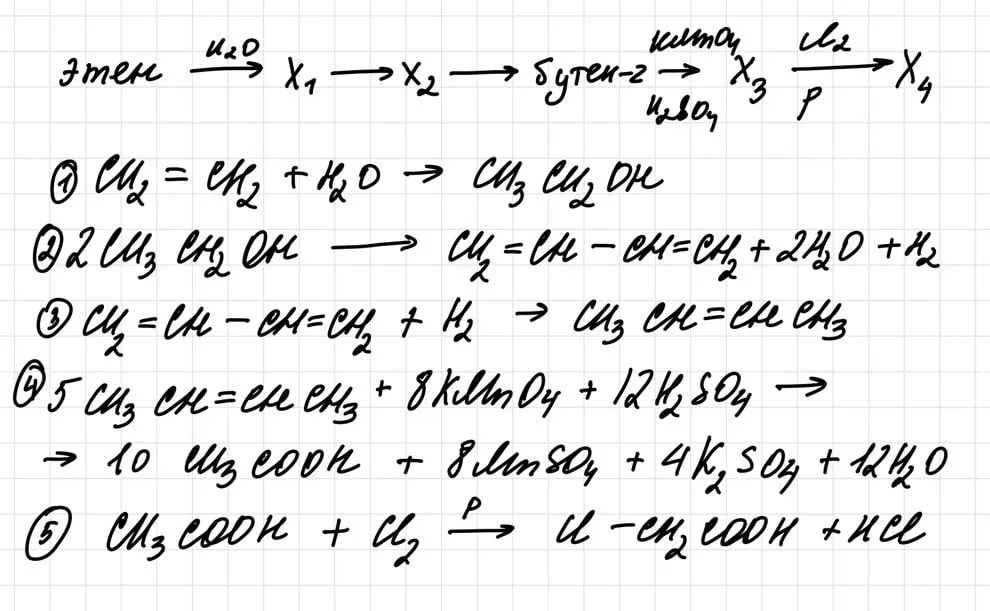
Катализатор в реакции Лебедева (вторая реакция) — смесь оксидов ZnO и Al₂O₃. Писать его необязательно, но это классная подсказка!
Задание 32: Дальний Восток ЕГЭ 2025
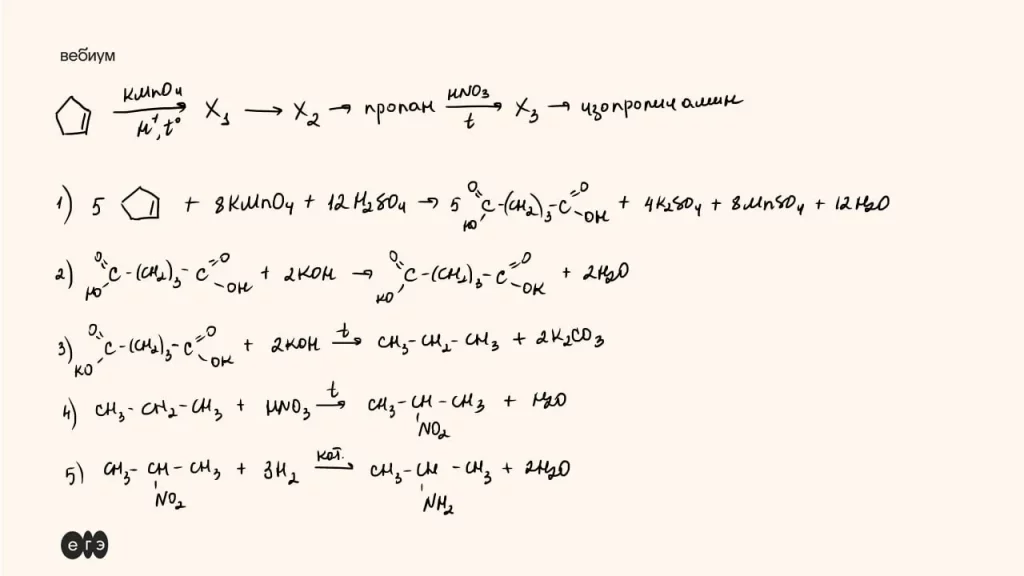
Задание 29: Дальний Восток ЕГЭ 2025
Вещества: перманганат калия, гидроксид калия, гидрокарбонат кальция, пероксид водорода, серная кислота, иодид калия
ОВР: образуется две соли, выделяется газ
5H₂O₂ + 2KMnO₄ + 3H₂SO₄ = 5O₂ + 2MnSO₄ + K₂SO₄ + 8H₂O
Задание 31: Дальний Восток ЕГЭ 2025
Магний поместили в разбавленный раствор азотной кислоты, в результате чего в растворе
образовалось две соли, а выделения газообразных продуктов не происходило. Получившуюся
соль магния выделили, высушили и прокалили. Образовавшееся простое вещество, взятое в
недостатке, вступило в реакцию с фосфором. Полученное соединение фосфора поместили в
концентрированный раствор азотной кислоты, при этом наблюдали выделение бурого газа.
1) 10HNO₃ + 4Mg = 4Mg(NO₃)₂ + NH4NO₃ + 3H₂O
2) 2Mg(NO₃)₂ = 2MgO + 4NO₂ + O₂
3) 4P + 3O₂ = 2P₂O₃
4) P₂O₃ + 4HNO₃ + H₂O = 2H₃PO₄ + 4NO₂
В избытке кислорода фосфор окисляется до P2O₅.
Напоминаю, что этот оксид может отщеплять воду от кислотных гидроксидов:
P₂O₅ + 2HNO₃ = 2HPO₃ + N₂O₅
Задание 34: Дальний Восток ЕГЭ 2025
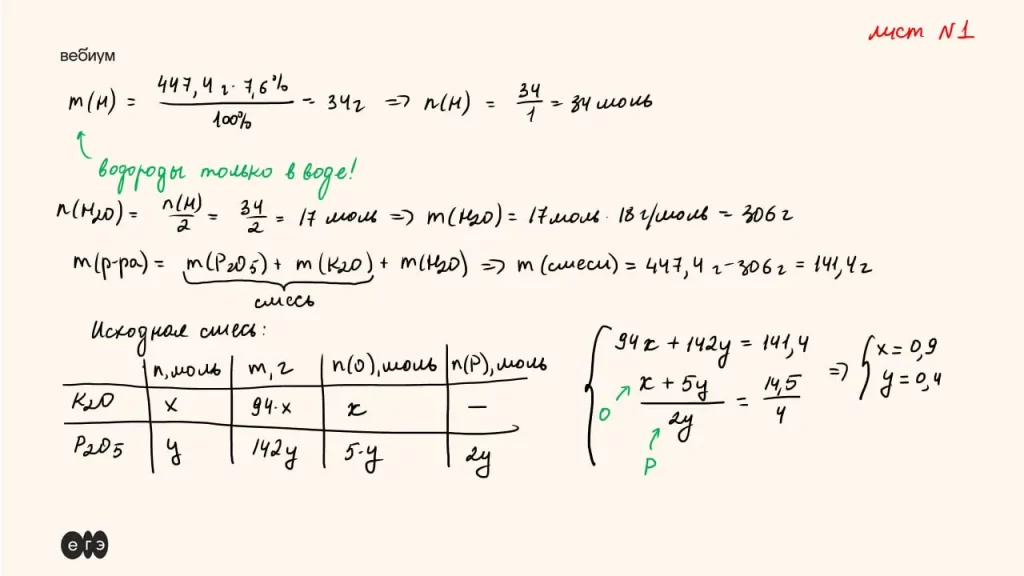

Смесь оксида фосфора (V) и оксида калия, в которой отношение атомов кислорода к числу атомов фосфора равно 14,5 : 4, сплавили. Образовавшуюся твердую смесь растворили в воде и получили 447,4 г раствора, в котором массовая доля атомов водорода равна 7,6%. Определите массу фосфата калия в полученном растворе.
P₂O₅ + 3K₂O = 2K₃PO₄
P₂O₅ + 3H₂O = 2H₃PO₄
2K₃PO₄ + H₃PO₄ = 3K₂HPO₄
Задание 34: Дальний Восток ЕГЭ 2025


К раствору аммиака массой 125 г с массовой долей протонов 56% добавили AlCl3 массой 40,05 г. К образовавшемуся раствору добавили сернистый газ, прореагировало 2,24 л. Вычислите массовые доли солей в конечном растворе.
3NH₃ + 3H₂O + AlCl₃ = 3NH₄Cl + Al(OH)₃
NH₃ + H₂O + SO₂ = NH₄HSO₃





Авторизуйтесь, чтобы оставить комментарий.